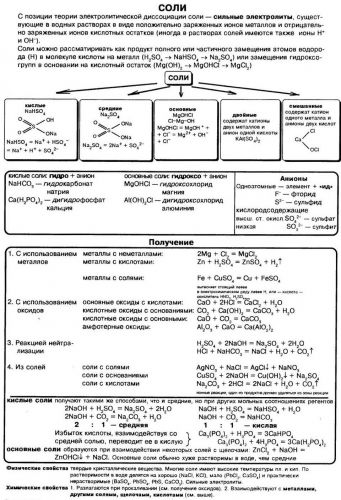
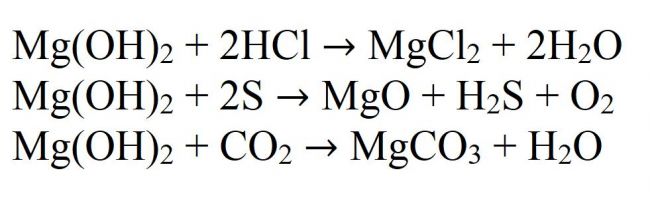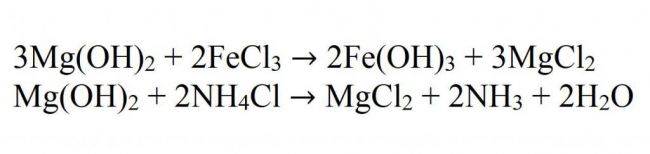Химические свойства оснований
Все основания подразделяют на:
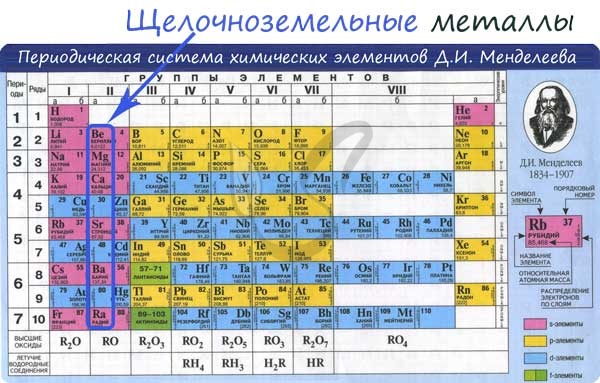
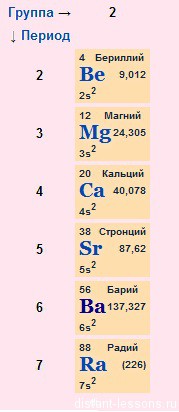
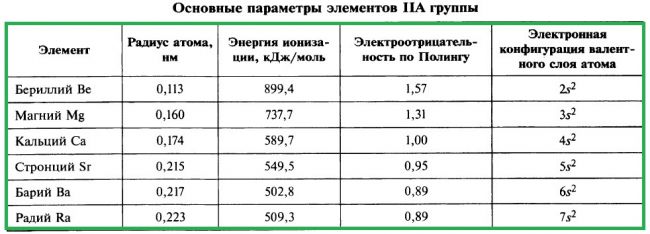
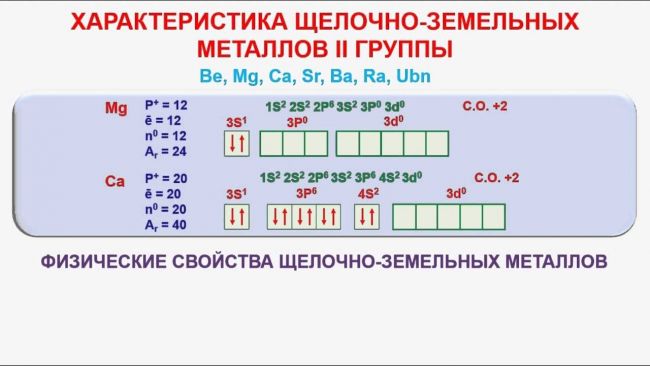
Напомним, что бериллий и магний к щелочноземельным металлам не относятся.
Помимо того, что щелочи растворимы в воде, они также очень хорошо диссоциируют в водных растворах, в то время как нерастворимые основания имеют низкую степень диссоциации.
Такое отличие в растворимости и способности к диссоциации у щелочей и нерастворимых гидроксидов приводит, в свою очередь, к заметным отличиям в их химических свойствах. Так, в частности, щелочи являются более химически активными соединениями и нередко способны вступать в те реакции, в которые не вступают нерастворимые основания.
Врачи отмечают, что щелочноземельные металлы играют важную роль в различных областях медицины и фармакологии. Эти элементы, такие как магний и кальций, необходимы для поддержания нормального функционирования организма. Например, магний участвует в метаболизме и помогает в поддержании здоровья сердечно-сосудистой системы. Кальций, в свою очередь, необходим для формирования костей и зубов, а также для нормальной работы мышц и нервов.
Однако специалисты предупреждают о потенциальных рисках, связанных с избыточным потреблением этих металлов. Некоторые исследования показывают, что высокие концентрации щелочноземельных металлов могут приводить к токсическим эффектам, особенно при длительном воздействии. Поэтому врачи рекомендуют соблюдать баланс и следить за уровнем этих элементов в организме, чтобы избежать негативных последствий для здоровья.

Взаимодействие оснований с кислотами
Щелочи реагируют абсолютно со всеми кислотами, даже очень слабыми и нерастворимыми. Например:
Нерастворимые основания реагируют практически со всеми растворимыми кислотами, не реагируют с нерастворимой кремниевой кислотой:
Следует отметить, что как сильные, так и слабые основания с общей формулой вида Me(OH)2 могут образовывать основные соли при недостатке кислоты, например:
Взаимодействие с кислотными оксидами
Щелочи реагируют со всеми кислотными оксидами, при этом образуются соли и часто вода:
Нерастворимые основания способны реагировать со всеми высшими кислотными оксидами, соответствующими устойчивым кислотам, например, P2O5, SO3, N2O5, с образованием средних солей:
<.p>
Нерастворимые основания вида Me(OH)2 реагируют в присутствии воды с углекислым газом исключительно с образованием основных солей. Например:
Cu(OH)2 + CO2 = (CuOH)2CO3 + H2O
С диоксидом кремния, ввиду его исключительной инертности, реагируют только самые сильные основания — щелочи. При этом образуются нормальные соли. С нерастворимыми основаниями реакция не идет. Например:
Щелочноземельные металлы вызывают интерес у ученых и промышленников благодаря своим уникальным свойствам. Многие отмечают их высокую реакцию с кислородом и водой, что делает их полезными в различных химических процессах. Например, магний и кальций активно используются в металлургии и строительстве. Некоторые эксперты подчеркивают важность этих металлов в производстве современных технологий, таких как аккумуляторы и магнитные материалы. Однако, несмотря на их полезность, существует и обеспокоенность по поводу экологических последствий добычи и переработки щелочноземельных металлов. Люди обсуждают необходимость разработки более устойчивых методов их извлечения, чтобы минимизировать воздействие на природу. В целом, щелочноземельные металлы остаются в центре внимания как в научных кругах, так и в промышленности, открывая новые горизонты для исследований и применения.

Взаимодействие оснований с амфотерными оксидами и гидроксидами
Все щелочи реагируют с амфотерными оксидами и гидроксидами. Если реакцию проводят, сплавляя амфотерный оксид либо гидроксид с твердой щелочью, такая реакция приводит к образованию безводородных солей:
Если же используют водные растворы щелочей, то образуются гидроксокомплексные соли:
В случае алюминия при действии избытка концентрированной щелочи вместо соли Na[Al(OH)4] образуется соль Na3[Al(OH)6]:
Взаимодействие оснований с солями
Какое-либо основание реагирует с какой-либо солью только при соблюдении одновременно двух условий:
1) растворимость исходных соединений;
2) наличие осадка или газа среди продуктов реакции
Например:

Термическая устойчивость оснований
Все щелочи, кроме Ca(OH)2, устойчивы к нагреванию и плавятся без разложения.
Все нерастворимые основания, а также малорастворимый Ca(OH)2 при нагревании разлагаются. Наиболее высокая температура разложения у гидроксида кальция – около 1000oC:
Нерастворимые гидроксиды имеют намного более низкие температуры разложения. Так, например, гидроксид меди (II) разлагается уже при температуре выше 70 oC:
Химические свойства амфотерных гидроксидов
Взаимодействие амфотерных гидроксидов с кислотами
Амфотерные гидроксиды реагируют с сильными кислотами:
Амфотерные гидроксиды металлов в степени окисления +3, т.е. вида Me(OH)3, не реагируют с такими кислотами, как H2S, H2SO3 и H2СO3 ввиду того, что соли, которые могли бы образоваться в результате таких реакций, подвержены необратимому гидролизу до исходного амфотерного гидроксида и соответствующей кислоты:
Взаимодействие амфотерных гидроксидов с кислотными оксидами
Амфотерные гидроксиды реагируют с высшими оксидами, которым соответствуют устойчивые кислоты (SO3, P2O5, N2O5):
Амфотерные гидроксиды металлов в степени окисления +3, т.е. вида Me(OH)3, не реагируют с кислотными оксидами SO2 и СO2.
Взаимодействие амфотерных гидроксидов с основаниями
Из оснований амфотерные гидроксиды реагируют только с щелочами. При этом, если используется водный раствор щелочи, то образуются гидроксокомплексные соли:
А при сплавлении амфотерных гидроксидов с твердыми щелочами получаются их безводные аналоги:
Амфотерные гидроксиды реагируют при сплавлении с оксидами щелочных и щелочноземельных металлов:
Термическое разложение амфотерных гидроксидов
Все амфотерные гидроксиды не растворимы в воде и, как любые нерастворимые гидроксиды, разлагаются при нагревании на соответствующий оксид и воду:
Применение:
Основная часть добываемого магния используется для получения различных легких сплавов. В состав этих сплавов, кроме магния, входят, как правило, алюминий, цинк, цирконий. Такие сплавы достаточно прочны и находят применение в самолетостроении, приборостроении и для других целей.
Для защиты от коррозии водонагревателей и отопительных котлов находят применение магниевые аноды, представляющие из себя стальные стержни с нанесенным на них слоем магниевого сплава. В этом случае разрушается сам анод, а не стенки водонагревателя (протекторная защита).
Высокая химическая активность металлического магния позволяет использовать его при магниетермическом получении таких металлов, как титан, цирконий, ванадий, уран и др. При этом магний реагирует с оксидом или фторидом получаемого металла, например:
2Mg + TiO2 = 2MgO + Ti или 2Mg + UF4 = 2MgF2 + U.
Широкое применение находят многие соединения магния, особенно его оксид, карбонат и сульфат. Так, горькая соль применяется в текстильной и бумажной промышленности, а также в медицине.
В человеческом организме количество магния составляет всего несколько десятых или сотых долей процента, однако он играет немаловажную роль в процессах жизнедеятельности. Магний усиливает процессы обмена углеводов в мышцах, регулирует обмен кальция; поэтому из-за недостатка магния развивается остеопороз и воспалительно-дистрофические заболевания опорно-двигательного аппарата.
Недостаточное количество магния в крови — признак переутомления или стрессового состояния. Доказано, что недостаток магния в организме способствует заболеванию инфарктом миокарда. В организм поступает с пищей, но при этом усваивается менее 40% магния, так как его соединения плохо всасываются кишечником.
Основным производителем этого металла в мире является Китай, который «монополизировал» мировой рынок. В 2007 году производство китайского магния достигло 260 тысяч тонн. В России производство сосредоточено в Пермском крае (25 тыс.т/год). В 2004 году создано ОАО «Русский магний» для строительства завода по производству магния в Асбесте (Свердловская область), но в настоящее время проект заморожен.
Алиуллов Андрей
ХФ ТюмГУ, 581 группа, 2011 г.
Химические свойства амфотерных оксидов цинка и алюминия
Рассмотрим амфотерные свойства оксидов цинка и алюминия. На примере их взаимодействия с основными и кислотными оксидами, с кислотой и щелочью.
— Взаимодействие с основными оксидами и основаниями:
ZnO + Na2O → Na2ZnO2 (цинкат натрия). Оксид цинка ведет себя как кислотный.
ZnO + 2NaOH → Na2ZnO2+ H2O
— Взаимодействие с кислотными оксидами и кислотами. Проявляет свойства основного оксида.
3ZnO + P2O5 → Zn3(PO4)2 (фосфат цинка)
ZnO + 2HCl → ZnCl2 + H2O
Аналогично оксиду цинка ведет себя и оксид алюминия:
— Взаимодействие с основными оксидами и основаниями:
Al2O3 + Na2O → 2NaAlO2 (метаалюминат натрия). Оксид алюминия ведет себя как кислотный.
Al2O3 + 2NaOH → 2NaAlO2+ H2O
— Взаимодействие с кислотными оксидами и кислотами. Проявляет свойства основного оксида.
Al2O3 + P2O5 → 2AlPO4(фосфат алюминия)
Al2O3 + 6HCl → 2AlCl3 + 3H2O
Рассмотренные реакции происходят при нагревании, при сплавлении. Если взять растворы веществ, то реакции пойдут несколько иначе.
Составить формулу оксидов.
При составлении формул оксида первым ставят элемент, степень окисления которого со знаком +, а вторым элемент с отрицательной степенью окисления. Для оксидов это всегда кислород.
Последующие действия по составлению формулы оксида:
1. Расставить степени окисления (степень окисления) для каждого атома. Кислород в оксидах всегда имеет степень окисления -2 (минус два).
2. Для того, чтобы правильно узнать степень окисления второго элемента, нужно заглянуть в таблицу возможных степеней окисления некоторых элементов.
|
Элемент |
Возможные степени окисления |
|---|---|
|
N (азот) |
-3, 0, +1, +2, +3, +4,+5. |
|
P (фосфор) |
-3, 0, +3, +5. |
|
S (сера) |
-2, 0, +4, +6. |
|
C (углерод) |
-4, 0, +2, +4. |
При составлении названий веществ чаще всего использую русские названия элементов, к примеру, дикислород, дифторид ксенона, селенат калия. Иногда для некоторых элементов в производные термины вводят корни их латинских наименований:
|
Ag — аргент |
N — нитр |
|---|---|
|
As — арс, арсен |
Ni — никкол |
|
Au — аур |
O — окс, оксиген |
|
C — карб, карбон |
Pb — плюмб |
|
Cu — купр |
S — сульф |
|
Fe — ферр |
Sb — стиб |
|
H — гидр, гидроген |
Si — сил, силик, силиц |
|
Hg — меркур |
Sn — станн |
|
Mn — манган |
К примеру: карбонат, манганат, оксид, сульфид, силикат.
Названия простых веществ состоят из одного слова — наименования химического элемента с числовой приставкой, например:
|
Mg — (моно)магний |
O3 — трикислород |
|---|---|
|
Hg — (моно) ртуть |
P4 — тетрафосфор |
|
O2 — дикислород |
S8 — октасера |
Используются следующие числовые приставки:
|
1 — моно |
7 — гепта |
|---|---|
|
2 — ди |
8 — окта |
|
3 — три |
9 — нона |
|
4 — тетра |
10 — дека |
|
5 — пента |
11 — ундека |
|
6 — гекса |
12 — додека |
Неопределенное число указывается числовой приставкой n — поли.
Названия распространенных кислотных гидроксидов состоят из двух слов: собственного названия с окончанием «ая» и группового слова «кислота». Приведем формулы и собственные названия распространенных кислотных гидроксидов и их кислотных остатков (прочерк означает, что гидроксид не известен в свободном виде или в кислом водном растворе):
|
Кислотный гидроксид |
Кислотный остаток |
|---|---|
|
HAsO2 — метамышьяковистая |
AsO2— — метаарсенит |
|
H3AsO3 — ортомышьяковистая |
AsO33- — ортоарсенит |
|
H3AsO4 — мышьяковая |
AsO43- — арсенат |
|
— |
В4О72- — тетраборат |
|
— |
ВiО3— — висмутат |
|
HBrO — бромноватистая |
BrO- — гипобромит |
|
HBrO3 — бромноватая |
BrO3— — бромат |
|
H2CO3 — угольная |
CO32- — карбонат |
|
HClO — хлорноватистая |
ClO— гипохлорит |
|
HClO2 — хлористая |
ClO2— хлорит |
|
HClO3 — хлорноватая |
ClO3— хлорат |
|
HClO4 — хлорная |
ClO4— перхлорат |
|
H2CrO4 — хромовая |
CrO42- — хромат |
|
— |
НCrO4— гидрохромат |
|
H2Cr2О7 — дихромовая |
Cr2O72- — дихромат |
|
— |
FeO42- — феррат |
|
HIO3 — иодноватая |
IO3— иодат |
|
HIO4 — метаиодная |
IO4— метапериодат |
|
H5IO6 — ортоиодная |
IO65- — ортопериодат |
|
HMnO4 — марганцовая |
MnO4— перманганат |
|
— |
MnO42- — манганат |
|
— |
MоO42- — молибдат |
|
HNO2 — азотистая |
NO2— нитрит |
|
HNO3 — азотная |
NO3— нитрат |
|
HPO3 — метафосфорная |
PO3— метафосфат |
|
H3PO4 — ортофосфорная |
PO43- — ортофосфат |
|
НPO42- — гидроортофосфат |
|
|
Н2PO4— дигидроотофосфат |
|
|
H4P2O7 — дифосфорная |
P2O74- — дифосфат |
|
— |
ReO4— перренат |
|
— |
SO32- — сульфит |
|
HSO3— гидросульфит |
|
|
H2SO4 — серная |
SO42- — сульфат |
|
— |
НSO4— гидросульфат |
|
H2S2O7 — дисерная |
S2O72- — дисульфат |
|
H2S2O6(O2) — пероксодисерная |
S2O6(O2)2- — пероксодисульфат |
|
H2SO3S — тиосерная |
SO3S2— тиосульфат |
|
H2SeO3 — селенистая |
SeO32- — селенит |
|
H2SeO4 — селеновая |
SeO42- — селенат |
|
H2SiO3 — метакремниевая |
SiO32- — метасиликат |
|
H4SiO4 — ортокремниевая |
SiO44- — ортосиликат |
|
H2TeO3 — теллуристая |
TeO32- — теллурит |
|
H2TeO4 — метателлуровая |
TeO42- — метателлурат |
|
H6TeO6 — ортотеллуровая |
TeO66- — ортотеллурат |
|
— |
VO3— метаванадат |
|
— |
VO43- — ортованадат |
|
— |
WO43- — вольфрамат |
Менее распространенные кислотные гидроксиды называют по номенклатурным правилам для комплексных соединений, например:
Химические свойства водорода
С точки зрения свойств водорода как простого вещества, он, все-таки, имеет больше общего с галогенами. Водород, также как и галогены, является неметаллом и образует аналогично им двухатомные молекулы (H2).
В обычных условиях водород представляет собой газообразное, малоактивное вещество. Невысокая активность водорода объясняется высокой прочностью связи между атомами водорода в молекуле, для разрыва которой требуется либо сильное нагревание, либо применение катализаторов, либо и то и другое одновременно.
Взаимодействие водорода с простыми веществами
с металлами
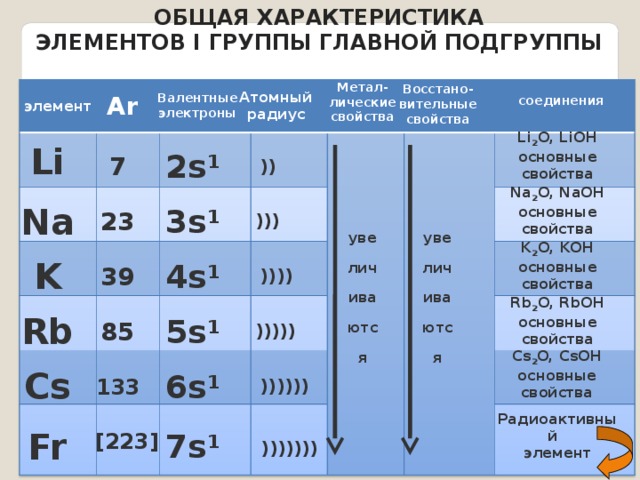
Из металлов водород реагирует только с щелочными и щелочноземельными! К щелочным металлам относятся металлы главной подгруппы I-й группы (Li, Na, K, Rb, Cs, Fr), а к щелочно-земельным — металлы главной подгруппы II-й группы, кроме бериллия и магния (Ca, Sr, Ba, Ra)
При взаимодействии с активными металлами водород проявляет окислительные свойства, т.е. понижает свою степень окисления. При этом образуются гидриды щелочных и щелочноземельных металлов, которые имеют ионное строение. Реакция протекает при нагревании:
Следует отметить, что взаимодействие с активными металлами является единственным случаем, когда молекулярный водород Н2 является окислителем.
с неметаллами
Из неметаллов водород реагирует только c углеродом, азотом, кислородом, серой, селеном и галогенами!
Под углеродом следует понимать графит или аморфный углерод, поскольку алмаз — крайне инертная аллотропная модификация углерода.
При взаимодействии с неметаллами водород может выполнять только функцию восстановителя, то есть только повышать свою степень окисления:
Взаимодействие водорода со сложными веществами
с оксидами металлов
Водород не реагирует с оксидами металлов, находящихся в ряду активности металлов до алюминия (включительно), однако, способен восстанавливать многие оксиды металлов правее алюминия при нагревании:
c оксидами неметаллов
Из оксидов неметаллов водород реагирует при нагревании с оксидами азота, галогенов и углерода. Из всех взаимодействий водорода с оксидами неметаллов особенно следует отметить его реакцию с угарным газом CO.
Смесь CO и H2 даже имеет свое собственное название – «синтез-газ», поскольку из нее в зависимости от условий могут быть получены такие востребованные продукты промышленности как метанол, формальдегид и даже синтетические углеводороды:
c кислотами
С неорганическими кислотами водород не реагирует!
Из органических кислот водород реагирует только с непредельными, а также с кислотами, содержащими функциональные группы способные к восстановлению водородом, в частности альдегидные, кето- или нитрогруппы.
c солями
В случае водных растворов солей их взаимодействие с водородом не протекает. Однако при пропускании водорода над твердыми солями некоторых металлов средней и низкой активности возможно их частичное или полное восстановление, например:
Какие оксиды реагируют с водой?
Из всех оксидов с водой реагируют только:
1) все активные основные оксиды (оксиды ЩМ и ЩЗМ);
2) все кислотные оксиды, кроме диоксида кремния (SiO2);
т.е. из вышесказанного следует, что с водой точно не реагируют:
1) все малоактивные основные оксиды;
2) все амфотерные оксиды;
3) несолеобразующие оксиды (NO, N2O, CO, SiO).
Примечание:
Оксид магния медленно реагирует с водой при кипячении. Без сильного нагревания реакция MgO с H2O не протекает.
Способность определить то, какие оксиды могут реагировать с водой даже без умения писать соответствующие уравнения реакций, уже позволяет получить баллы за некоторые вопросы тестовой части ЕГЭ.
Теперь давайте разберемся, как же все-таки те или иные оксиды реагируют с водой, т.е. научимся писать соответствующие уравнения реакций.
Активные основные оксиды, реагируя с водой, образуют соответствующие им гидроксиды. Напомним, что соответствующим оксиду металла является такой гидроксид, который содержит металл в той же степени окисления, что и оксид. Так, например, при реакции с водой активных основных оксидов K+12O и Ba+2O образуются соответствующие им гидроксиды K+1OH и Ba+2(OH)2:
K2O + H2O = 2KOH – гидроксид калия
BaO + H2O = Ba(OH)2 – гидроксид бария
Все гидроксиды, соответствующие активным основным оксидам (оксидам ЩМ и ЩЗМ), относятся к щелочам. Щелочами называют все хорошо растворимые в воде гидроксиды металлов, а также малорастворимый гидроксид кальция Ca(OH)2 (как исключение).
Взаимодействие кислотных оксидов с водой так же, как и реакция активных основных оксидов с водой, приводит к образованию соответствующих гидроксидов. Только в случае кислотных оксидов им соответствуют не основные, а кислотные гидроксиды, чаще называемые кислородсодержащими кислотами. Напомним, что соответствующей кислотному оксиду является такая кислородсодержащая кислота, которая содержит кислотообразующий элемент в той же степени окисления, что и в оксиде.
Таким образом, если мы, например, хотим записать уравнение взаимодействия кислотного оксида SO3 с водой, прежде всего мы должны вспомнить основные, изучаемые в рамках школьной программы, серосодержащие кислоты. Таковыми являются сероводородная H2S, сернистая H2SO3 и серная H2SO4 кислоты. Cероводородная кислота H2S, как легко заметить, не является кислородсодержащей, поэтому ее образование при взаимодействии SO3 с водой можно сразу исключить. Из кислот H2SO3 и H2SO4 серу в степени окисления +6, как в оксиде SO3, содержит только серная кислота H2SO4. Поэтому именно она и будет образовываться в реакции SO3 с водой:
H2O + SO3 = H2SO4
Аналогично оксид N2O5, содержащий азот в степени окисления +5, реагируя с водой, образует азотную кислоту HNO3, но ни в коем случае не азотистую HNO2, поскольку в азотной кислоте степень окисления азота, как и в N2O5, равна +5, а в азотистой — +3:
N+52O5 + H2O = 2HN+5O3
Исключение:
Оксид азота (IV) (NO2) является оксидом неметалла в степени окисления +4, т.е. в соответствии с алгоритмом, описанным в таблице в самом начале данной главы, его нужно отнести к кислотным оксидам. Однако не существует такой кислоты, которая содержала бы азот в степени окисления +4.
В случае оксида NO2 принято считать, что ему соответствуют сразу две кислоты, поскольку его взаимодействие с водой приводит к одновременному образованию двух кислот:
2NO2 + H2O = HNO2 + HNO3
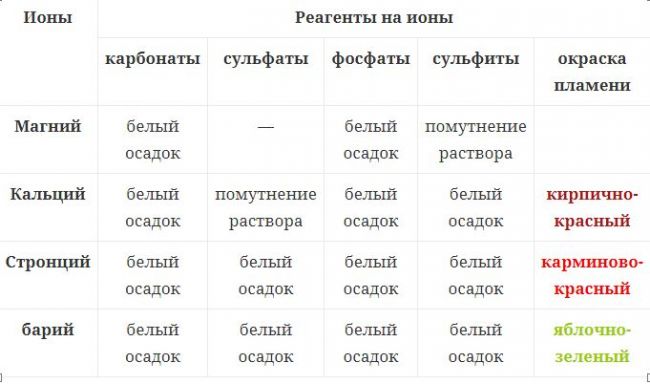
Распространение в природе
Гидроксид магния в природе встречается в виде минерала брусита. Крупные месторождения этой породы — большая редкость. В России его добывают на Кульдурском месторождении, где его запасы оценивают в 14 миллионов тонн. Добыча на нем идет со скоростью примерно в 250 тысяч тонн продукта в год, но с этого года объемы добычи увеличились вдвое. Причиной этому стал хороший спрос на этот минерал за границей. Самым крупным импортером является Япония.
Выглядит брусит как белые, серые или зеленовато-белые кристаллы со стеклянным блеском на изломе. Имеет довольно низкую твердость, поэтому легко режется ножом. Может содержать примеси. В зависимости от их количества и типа выделяют несколько подвидов этого минерала. Так, ферронемалит содержит в себе, помимо гидроксида магния, 5 % железа в виде оксида, а ферробрусит — уже целых 36 %. Оксид железа имеет бурый цвет (цвет ржавчины), поэтому эти минералы приобретают тот же оттенок вместо привычного светло-зеленого. Существует еще и мангобрусит. В качестве примеси здесь выступает марганец. Такой минерал имеет уже медово-желтый цвет. Но при контакте с кислородом воздуха минерал быстро теряет свой красивый цвет и быстро чернеет.
Применяют данный минерал в основном как сырье. Из него получают оксид и другие соединения магния, флюсы, различные огнеупорные материалы. Но брусит можно применять и без какой-либо обработки. Так, этот минерал используют для очистки газов от хлора и для сорбционного фильтрования воды.
Химические свойства
Гидроксид магния — типичное нерастворимое основание. Это и определяет его химические свойства. Так, например, реагирует гидроксид магния с кислотами, кислотными оксидами и неметаллами:
Из-за последней реакции он имеет склонность поглощать углекислый газ прямо из воздуха с образованием карбоната, поэтому хранить данное вещество длительное время открытым не рекомендуется.
Взаимодействует также и с солями, если в результате реакции получается осадок или газ:
Как уже было указано выше, при нагревании идет разложение гидроксида магния по уравнению:
Mg(OH)2 → H2O + MgO
Что касается образования комплексных соединений, где катион магния выступал бы в качестве лиганда, то на этот счет имеются противоречивые сведения. В одних источниках указывается, что магний не склонен к их образованию, и существуют лишь только неустойчивые соединения с галогенидами магния. В других источниках указывается, что гидроксид магния может реагировать с горячими щелочами с образованием гидромагнезатов:
Mg(OH)2 + 2NaOH → Na2[Mg(OH)4]
Химические свойства фосфора
Существует несколько аллотропных модификаций фосфора., в частности белый фосфор, красный фосфор и черный фосфор.
Белый фосфор образован четырехатомными молекулами P4, не является устойчивой модификацией фосфора. Ядовит. При комнатной температуре мягкий и подобно воску легко режется ножом. На воздухе медленно окисляется, и из-за особенностей механизма такого окисления светится в темноте (явление хемилюминесценции). Даже при слабом нагревании возможно самопроизвольное воспламенение белого фосфора.
Из всех аллотропных модификаций белый фосфор наиболее активен.
Красный фосфор состоит из длинных молекул переменного состава Pn. В некоторых источниках указывается то, что он имеет атомное строение, но корректнее все-таки считать его строение молекулярным. Вследствие особенностей строения является менее активным веществом по сравнению с белым фосфором, в частности в отличие от белого фосфора на воздухе окисляется значительно медленнее и для его воспламенения требуется поджиг.
Черный фосфор состоит из непрерывных цепей Pn и имеет слоистую структуру схожую со структурой графита, из-за чего и внешне похож на него. Данная аллотропная модификация имеет атомное строение. Самый устойчивый из всех аллотропных модификаций фосфора, наиболее химически пассивен. По этой причине, рассмотренные ниже химические свойства фосфора следует относить прежде всего к белому и красному фосфору.
Взаимодействие фосфора с неметаллами
Реакционная способность фосфора является более высокой, чем у азота. Так, фосфор способен гореть после поджига при обычных условиях, образуя кислотный оксид Р2O5:
а при недостатке кислорода оксид фосфора (III):
Реакция с галогенами также протекает интенсивно. Так, при хлорировании и бромировании фосфора в зависимости от пропорций реагентов образуются тригалогениды или пентагалогениды фосфора:
Ввиду существенно более слабых окислительных свойства йода по сравнению с остальными галогенами, возможно окисление фосфора йодом только до степени окисления +3:
В отличие от азота фосфор с водородом не реагирует.
Взаимодействие фосфора с металлами
Фосфор реагирует при нагревании с активными металлами и металлами средней активности образуя фосфиды:
Фосфиды активных металлов подобно нитридам гидролизуются водой:
А также водными растворами кислот-неокислителей:
Взаимодействие фосфора со сложными веществами
Фосфор окисляется кислотами окислителями, в частности, концентрированными азотной и серной кислотами:
Следует знать, что белый фосфор реагирует с водными растворами щелочей. Однако, ввиду специфичности умение записывать уравнения таких взаимодействий на ЕГЭ по химии пока еще не требовалось.
Тем не менее, тем, кто претендует на 100 баллов, для собственного спокойствия, можно запомнить следующие особенности взаимодействия фосфора с растворами щелочей на холоду и при нагревании.
На холоду взаимодействие белого фосфора с растворами щелочей протекает медленно. Реакция сопровождается образованием газа с запахом тухлой рыбы — фосфина и соединения с редкой степенью окисления фосфора +1:
При взаимодействии белого фосфора с концентрированным раствором щелочи при кипячении выделяется водород и образуется фосфит:
Химические свойства:
Отношение к воздуху и кислороду при обычных условиях: …
При нагревании: …
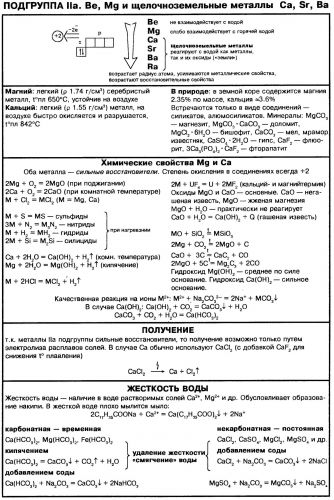
С холодной водой магний почти не взаимодействует, но при нагревании разлагает ее с выделением водорода. В этом отношении он занимает промежуточное положение между бериллием, который вообще с водой не реагирует и кальцием, легко с ней взаимодействующим.
В электрохимическом ряду напряжений магний стоит значительно левее водорода и активно реагирует с разбавленными кислотами с образованием солей. В этих реакциях есть у магния особенности. Он не растворяется во фтороводородной, концентрированной серной и в смеси серной и в смеси азотной кислот, растворяющей другие металлы почти столь же эффективно, как «царская водка» (смесь HCl и HNO3). Не взаимодействует с растворами щелочей.
Гидроксид магния. Фармакологические свойства
Гидроксид магния нейтрализует в желудочном соке свободную соляную кислоту с образованием хлорида магния. Далее хлорид магния переходит в кишечник, где, действуя как солевое слабительное, оказывает послабляющий эффект (плохо всасывается, повышает в просвете кишечника осмотическое давление, способствует переходу жидкости по градиенту концентрации, увеличивает объемы кишечного содержимого, которое растягивает стенки кишечника и стимулирует его перистальтику). Выводятся ионы магния в виде водорастворимых солей (бикарбоната и хлорида) и малорастворимой гидроокиси с содержимым кишечника. Гидроксид магния связывает желчные кислоты и инактивирует пепсин, которые попадают в результате рефлюкса из двенадцатиперстной кишки в желудок, тем самым оказывает защитное воздействие на слизистую оболочку двенадцатиперстной кишки и желудка, в том числе и при язвенной болезни. В желудке гидроксид магния не сразу расходуется и может нейтрализовать соляную кислоту, которая выделяется через некоторое время после употребления препарата. Таким образом, гидроксид магния характеризуется быстрым и продолжительным антацидным эффектом, не сопровождающимся изменениями кислотно-щелочного состояния и вторичной гиперсекрецией соляной кислоты. Гидроксид магния повышает перистальтику во всех отделах кишечника. Слабительное действие гидроксида магния наступает через 0,5–6 часов. При применении гидроксида магния у больных с нарушениями работы почек возможно поступления небольшого количества магния в кровь и развитие токсических реакций, которые проявляются угнетением центральной нервной системы.
Вопрос-ответ
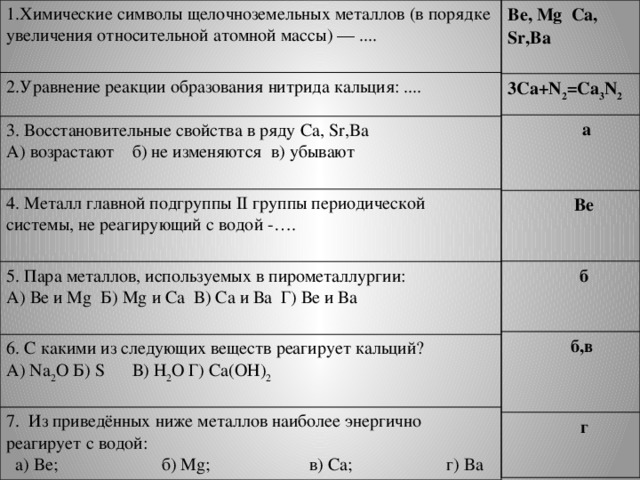
Как распознать щелочноземельные металлы?
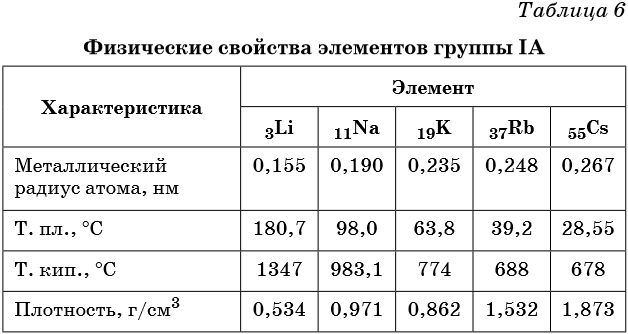
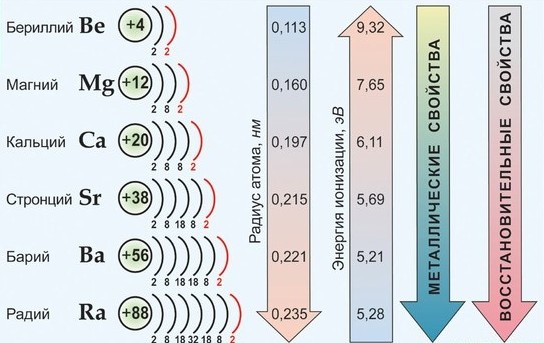
Все щёлочноземельные металлы серые, твёрдые при комнатной температуре вещества. В отличие от щелочных металлов, они существенно более твёрдые, и ножом преимущественно не режутся (исключение — стронций). Самый тяжёлый — радий, по плотности сравнимый с германием.
Какие элементы являются щелочными металлами?
Щелочны́е мета́ллы — элементы 1-й группы периодической таблицы химических элементов (по устаревшей классификации — элементы главной подгруппы I группы): литий Li, натрий Na, калий K, рубидий Rb, цезий Cs, франций Fr.
Что образуют щелочноземельные металлы с водой?
Щелочноземельные металлы при их взаимодействии (или их оксидов) с водой образуют основные гидроксиды (основания). Сила оснований увеличивается в группе сверху вниз. Гидроксиды щелочноземельных металлов являются сильными основаниями, растворимыми в воде — щелочами.
Как можно получить щелочноземельные металлы?
Щелочноземельные металлы получают в основном электролизом расплавов галогенидов. Чаще используются хлориды металлов. При этом на катоде восстанавливаются катионы, а на аноде окисляются анионы.
Советы
СОВЕТ №1
Изучите основные свойства щелочноземельных металлов, такие как высокая реакционная способность и низкая плотность. Это поможет вам лучше понять их поведение в различных химических реакциях и их применение в промышленности.
СОВЕТ №2
Обратите внимание на безопасность при работе с щелочноземельными металлами. Из-за их высокой реактивности, особенно с водой и кислородом, важно использовать соответствующие средства защиты и соблюдать осторожность.
СОВЕТ №3
Исследуйте различные области применения щелочноземельных металлов, такие как производство магнитов, фосфоров для освещения и катализаторов. Это поможет вам понять их значимость в современных технологиях и науке.
СОВЕТ №4
Следите за последними исследованиями и разработками в области щелочноземельных металлов. Научные открытия могут открывать новые возможности для их использования и улучшения существующих технологий.